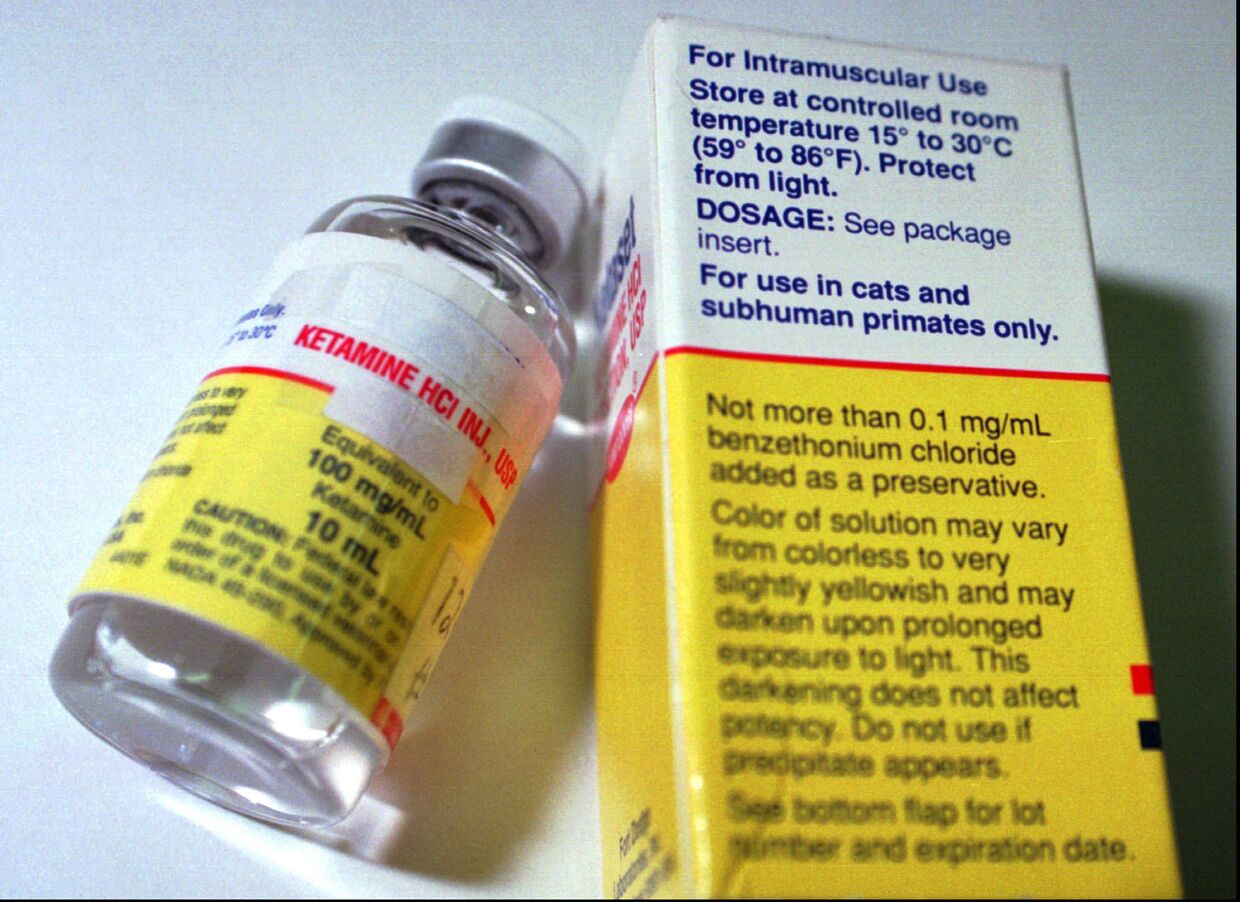
Поразительный эффект кетамина подкрепляет новую теорию психических заболеваний.
В один из солнечных дней этой осени мне довелось стать свидетелем новой методики лечения психических заболеваний. В психиатрической клинике близ Йельского университета страдавшему от депрессии пациенту вводили кетамин. На протяжении 40 минут препарат через вену поступал в кровь, а затем к клеткам головного мозга. Если его эффект подтвердится, кетамин станет первым препаратом, способным быстро остановить суицидальные побуждения и потенциально спасти много жизней. В других исследованиях вызываемый кетамином эффект рассматривают как вакцинацию против депрессии и посттравматического стресса. А по сути, цель заключается не в чем ином, как в пересмотре нашего понимания самой природы психических заболеваний.
Депрессия — наиболее распространенное психическое заболевание в Соединенных Штатах, которому в разные моменты своей жизни подвержено 30% американцев. Однако, несмотря на полвека исследований, повсеместную рекламу и невероятные объемы продаж, антидепрессанты просто-напросто не очень эффективны. Они лечат депрессию так, будто она была вызвана химическим дисбалансом: закачать побольше одного компонента или впитать другого, и проблема решена.
Но взаимодействие между этими химическими веществами (взять тот же серотонин) и депрессией оказывается относительно слабым. Возникшая недавно конкурирующая теория, отчасти вдохновленная эффективностью кетамина, гласит, что психические заболевания обусловлены не столько химическим дисбалансом, сколько структурными изменениями в головном мозге — и что основной причиной этих изменений является психологический стресс. «Я действительно думаю, что стресс ведет к психическим заболеваниям, как сигареты — к болезням сердца», — говорит Джерард Санакора (Gerard Sanacora), профессор психиатрии, проводящий испытания кетамина в Йельском университете.
В соответствии с этой теорией, стресс постепенно стачивает отдельные нейроны, подобно тому, как ливни точат кровлю. Это, в свою очередь, ведет к изменению характера их взаимных соединений и структуры мозга. Кетамин, наряду с некоторыми подобными ему молекулами, помогает укрепить нейроны против этих повреждений, влияя не только на химию мозга, но и на его структуру.
Психиатрические больницы, как правило, не наблюдают пациентов до их срыва: мозг, сформированный уязвимыми генами и разрушенный стрессом от потери или травмы. В случае с другими заболеваниями, такими как болезни сердца, рак, СПИД, все работает по-другому. На ранних стадиях их можно взять под контроль и предотвратить кризисы.

Если предположения Санакоры и его единомышленников оправдаются, мы можем оказаться на пороге кардинальных изменений, которые позволят применять аналогичный подход к психическим заболеваниям. А он, в свою очередь, может с помощью своеобразной прививки рассудку предотвратить психическое расстройство, прежде чем оно поразит человека.
Необходимость в прогрессе едва ли могла быть более актуальной: по оценкам, из всех болезней нервно-психические заболевания висят на обществе самым тяжелым бременем. Почти половина американцев в определенный момент своей жизни страдает от какой-либо формы психического расстройства. Самоубийства, 90% которых совершают душевнобольные, ежегодно уносят в Америке 40 тысяч жизней — цифра, превышающая число убийств или смертей в автомобильных авариях. С 2005 года число самоубийств среди американских участников боевых действий выросло почти в два раза, в первой половине 2012 года в результате самоубийств погибло больше военнослужащих, чем в бою. Немного найдется медицинских неудач, сравнимых по грубости с неспособностью психиатрии спасти этих людей.
В то же время лечение может быть крайне неэффективным. По данным исследования 2006 STAR*D, крупнейшего клинического испытания антидепрессантов, менее трети страдающих депрессией пациентов реагируют на лекарства в течение 14 недель. После шести месяцев лечения несколькими препаратами выздоравливает только половина пациентов. 33% не реагирует вообще ни на одно лекарство. Даже если таблетки работают, это происходит медленно — смертельный риск, учитывая, что люди с аффективными расстройствами убивают себя чаще, чем кто-либо другой.
Наши способы лечения не эффективны отчасти потому, что мы на самом деле не понимаем, как они работают. Серотонин, в настоящее время наиболее распространенная мишень для антидепрессантов, — нейромедиатор, химическое вещество, которое разносит по головному мозгу разнообразные сообщения. Однако впервые он был найден в 1935 году в кишечнике. Название «серотонин» происходит от названия сыворотки крови (blood serum), благодаря которой ученые Кливлендcкой клиники открыли это вещество в 1948 году, отмечая, что это оно помогает свертыванию.
Когда 25-летняя аспирантка Гарварда Бетти Твэрег (Betty Twarog) позднее обнаружила серотонин в нейронах, ее открытие никто не воспринял всерьез. В то время сигналы мозга считались чисто электрическими импульсами, скачущими между клетками. Как рассказывает в своей книге «Массовое производство депрессии» Гэри Гринберг (Gary Greenberg), Твэрег назвала эту старую идею «полнейшим интеллектуальным идиотизмом». Работая в Кливлендской клинике в 1953 году, она нашла серотонин в мозге крыс, собак и обезьян.
Твэрег еще не знала, что там делает серотонин, но ключ к решению вскоре нашел Д.В. Вулли (D.W. Woolley), биохимик из Университета Рокфеллера в Нью-Йорке. В 1954 году Вулли в одной из своих работ указал на то, что диэтиламид лизергиновой кислоты, или ЛСД, химически похож на серотонин и аналогичным образом обрабатывается в головном мозге. Поскольку ЛСД «вызывает у человека психические нарушения, напоминающие шизофрению», написал он, другой препарат, влияя на серотонин, может быть использован для лечения шизофрении. Работе Твэрег потребовались бы годы, чтобы просочиться через научную область, где доминируют мужчины, но ее работу вместе с исследованием Вулли станут воспринимать как свидетельство того, насколько могут быть важны химические вещества, подобные серотонину, для системы сигналов головного мозга. Это открытие было прорывом в неврологии, но оно в то же время породило устойчивое заблуждение, касающееся психической болезни. «Тезис этой работы,— писал Вулли, — в том, что… серотонин играет важную роль в психических процессах, и ослабление его воздействия приводит к психическому расстройству. Другими словами, именно нехватка серотонина является причиной расстройства».
Примерно в то же время другие исследователи случайно наткнулись на первые антидепрессанты, ипрониазид и имипрамин. Предназначенные для лечения туберкулеза и шизофрении соответственно, эти препараты также вызывали у некоторых пациентов чувство «неуместного счастья». Исследователи обнаружили, что данные препараты повышали уровень серотонина, наряду с соответствующими нейротрансмиттерами. С этого момента начались усиленные поиски химически аналогичных препаратов, которые бы работали лучше в качестве антидепрессантов.

Ипрониазид был первым из этой группы лекарственных средств, блокирующих фермент, который разрушает серотонин, к ним также относятся два других нейротрансмиттера — допамин и норэпинефрин. Главный недостаток этих препаратов, называемых ингибиторами моноаминоксидазы (ИМАО), заключается в том, что они требуют строгой диеты: никаких зрелых сыров, вина, пива или колбас. В сочетании с этими продуктами препараты могут вызвать смертельно опасные скачки артериального давления — морока, из-за которой многие пациенты бросают их принимать (писатель Дэвид Фостер Уоллес (David Foster Wallac) на протяжении десятилетий принимал эти препараты, а спустя несколько месяцев после того, как слез с антидепрессантов — отчасти для того, чтобы избежать ограничений в питании — покончил жизнь самоубийством). С другой стороны, трициклические антидепрессанты, такие как имипрамин, блокируют реабсорбцию серотонина и норадреналина. Расплачиваться приходится множеством побочных эффектов: от сухости во рту и набора веса до эректильной дисфункции и потери либидо.
Следующее поколение препаратов ориентировалось на более тонкую настройку тех же механизмов и несколько уменьшило побочные эффекты. Новый класс препаратов, известных как селективные ингибиторы обратного захвата серотонина (СИОЗС), возник в 80-е годы, к таким лекарствам, как Prozac, Zoloft и Paxil пришел невероятный коммерческий успех. Поскольку СИОЗС сосредоточены конкретно на серотонине, их представляли как более целенаправленные варианты, между тем, они не намного эффективнее для подъема настроения, чем прежние препараты. Мы часто воспринимаем депрессию как естественную аналогию диабету: если вы находитесь в депрессии, это потому, что вам нужен серотонин, как диабетику нужен инсулин. Фармацевтические компании часто говорят, что аффективные расстройства обусловлены «химическим дисбалансом» серотонина или подобным ему веществом. В одной из реклам Zoloft, лидера продаж среди антидепрессантов, показан печальный белый круг, мило ползущий под серым облаком, а голос за кадром заверяет, что депрессия может быть «связана с дисбалансом естественных химических веществ в головном мозге». «Zoloft способен исправить этот дисбаланс».
Однако доказательство этому — довольно слабое. Prozac повышает уровень серотонина в течение нескольких часов, но неделями не меняет настроения. Когда ученые резко сокращают количество серотонина у здоровых людей, это не вгоняет их в тоску. А когда врачи измеряют уровень серотонина в спинномозговой жидкости людей, страдающих депрессией, они не обнаруживают там последовательного дефицита. Одно исследование 2008 года даже зарегистрировало повышенные уровни серотонина в мозге депрессивных людей. Лекарственный препарат тианептин, разработанный в конце 80-х годов, снижает уровень серотонина и все же снимает депрессию. К тому же исследования показали, что у влюбленных уровень серотонина ниже, а не выше.
Очевидно, что серотонин — не просто вещество, заставляющее чувствовать себя хорошо. Если препарат на основе серотонина, например, Zoloft, делает вас счастливее, то работает он каким-то другим, косвенным образом. Как в 2011 году заявил психиатр Рональд Пайз (Ronald Pies), редактор Psychiatric Times: «Понятие „химического дисбаланса“ всегда было своего рода городской легендой — и никогда теорией, серьезно выдвигаемой хорошо информированными психиатрами».
В то время как серотонин сильно не дотягивает до основательного объяснения депрессии, возникает более вероятный кандидат.
Стресс в меру не вреден, а способен мотивировать. Кортизол, гормон стресса, циркулирует ежедневно. Синхронизированный с солнечным светом, он помогает нам пробуждаться с утра. У здорового человека этот гормон особенно активизируется, когда требуется концентрация внимания: тест, собеседование, свидание. Исследования грызунов и человека подтверждают, что краткие, незначительные потрясения оказывают благоприятное воздействие на мозг, в частности, на память. Во время этих скачков рождаются нейроны и распространяются в гиппокампе, отделе мозга в форме морского конька, который ответственен за формирование новых воспоминаний и понимание трехмерного пространства, и грызуны учатся лучше. Студент, испытывающий стресс во время учебы, более внимателен и помнит больше, чем тот, кто не столь бдителен. Проблема возникает тогда, когда стресс в определенный момент или слишком интенсивен, как при изнасиловании или насильственном нападении, или слишком устойчив, как при длительной нищете, отсутствии заботы или плохом обращении.
В зависимости от продолжительности стресс по-разному меняет структуру мозга. В результате хронического стресса, например, детской травмы, гормоны начинают оказывать на клетки головного мозга обратный эффект: нейроны гиппокампа и префронтальной коры, отвечающей за настроение и управление импульсами, начинают сокращаться, в то время как цепочки нейронов в мозжечковой миндалине, где рождаются наши ощущения страха и тревоги, ширятся, как разросшийся кустарник. Но у каждого человека своя степень уязвимости, обусловленная генами и предшествующим жизненным опытом. «Если взять двух человек и подвергнуть их одной и той же стрессовой ситуации, для одного из них она будет пагубна, тогда как для другого — нет, — говорит Маурицио Пополи (Maurizio Popoli), профессор фармакологии в Миланском университете. — Это связано с тем, что они по-разному воспринимают стресс».
Наиболее важный эффект гормонов стресса заключается в том, чтобы затопить части мозга глутаматом, сигналом «к действию». Используемый 80% нейронов в коре головного мозга, этот ключевой нейромедиатор управляет психическими процессами: начиная с памяти и заканчивая настроением. Глутамат заставляет нейроны генерировать неожиданные всплески электроэнергии, которые высвобождают еще больше глутамата, а он в свою очередь вызывает электрические всплески в близлежащих нейронах.
Эту клеточную связь называют возбуждением, и она служит основой обработки информации в мозге. Как и у сексуальной возбудимости, у нее есть приливы и отливы; за каждым взрывом, или скачком, нейрона следует «рефрактерная фаза», в течение которой нейрон не может быть возбужден. Другие нейромедиаторы, такие как серотонин, называются «модулирующими», поскольку они изменяют чувствительность нейронов, которые секретируют глутамат (среди прочих). Сигналы этими модуляторами передает менее одного процента нейронов в коре головного мозга. Как выразился Пополи, эти модуляторы «крайне важны для тонкой настройки механизма. Но сам этот механизм является машиной возбудимости», движимой глутаматом.
Глутамат передвигается между нейронами подобно кораблю. Море, по которому он плывет, называется синапс, берег, от которого он отчаливает, — это пресинаптический нейрон, а пунктом назначения, на противоположной стороне синапса, служит постсинаптический нейрон. Еще один компонент, называемый глиальной клеткой, работает, чтобы удалить суда глутамата из синапса и утилизировать их. На каждом из этих этапов система глутамата оказывается под влиянием гормонов стресса: они заставляют первый нейрон отправлять больше судов, мешают утилизации глиальными клетками и блокируют доки на дальнем берегу. Все эти изменения увеличивают количество глутаматных кораблей, оставшихся в синапсе, перегружая клетки искаженными сигналами. В самом деле, мозг людей, страдающих депрессией, или по крайней мере модели депрессии у животных, выявляют все эти три проблемы, приводящие к длительному переизбытку глутамата в ключевых участках мозга.
Эти излишки глутамата заставляют нейроны вспыхивать раньше, чем следует, и запускают каскад сигналов внутри клетки, повреждая ее структуру. Глутамат связывается с нейроном и позволяет проникнуть внутрь потоку положительно заряженных частиц, в том числе кальция, жизненно важных для возбуждения нейронов. Но будучи в избытке, кальций активирует ферменты, разрушающие нейроны. Каждый нейрон имеет древовидные ветви, называемые дендритами, которые используются для связи с другими нейронами. При передозировке глутамата этот шатер из веток сморщивается, как растение, облитое гербицидом. Сначала исчезают «веточки», называемые шипиками. После длительного стресса отмирает целое разветвление.
Считается, что этот вредоносный процесс, называемый эксайтотоксичность, участвует в биполярном расстройстве, депрессии, эпилепсии и нейродегенеративных заболеваниях, таких как болезнь Альцгеймера, Хантингтона и Паркинсона. При депрессии многие зоны головного мозга усыхают и теряют активность, в том числе часть префронтальной коры и гиппокамп. Санакора и его коллеги полагают, что изменения в мозге, вызывающие аффективные расстройства, отчасти проистекают из хронического стресса нейронов, перевозбужденных глутаматом.
Как правило, мы склонны рассматривать приспособляемость нашего мозга как положительное качество. По мере того как нейроны растут в период развития, мозговая «проводка» у взрослого человека может меняться. После ударов или других травм головного мозга нейронные сигналы перенаправляют самих себя, позволяя даже очень старым людям заново обрести потерянные навыки. Психотерапия и медитация способны изменить шаблоны мозговой деятельности, так что в процессе лечения человек их полностью усваивает.
Однако нейропластическая гипотеза психического расстройства выявляет недостаток такого нейронного либерализма: гибкость человеческого мозга не только дает шанс на регенерацию, но и делает его уязвимым и легко изменяемым под воздействием стресса. После травмы, полученной на войне, тяжелого разрыва отношений или приступа одиночества человек с соответствующей генетической предрасположенностью может обнаружить, что его разум оказался в петле хронического страха или депрессии.
Широко используемые сегодня препараты для повышения настроения сосредоточены на модуляторных нейротрансмиттерах, подобных серотонину. Кетамин, между тем, оказывает непосредственное влияние на передачу сигналов глутаматом. Если кетамин нащупывает корень проблемы, это могло бы объяснить, почему он работает быстрее, лучше и чаще, чем более популярные антидепрессанты.
Не все согласны с идеей о том, что глутамат и стресс занимают центральное место при депрессии. Некоторые эксперты видят в воздействии стресса нижележащие эффекты, а не первопричину аффективных расстройств. «Механизм действия хорошего лечения не должен в обратном порядке повторять механизм заболевания», — говорит Эрик Нестлер (Eric Nestler), специалист по зависимостям и депрессии в Mt. Sinai Hospital. Препараты на основе серотонина и кетамин могут повлиять на депрессию косвенно, даже если аномалии с серотонином или глутаматом являются корнем депрессии. Нестлер также указывает на то, что депрессия, вероятно, включает в себя целое разнообразие подтипов, у которых нет какой-то причины. Он рассматривает депрессию не как единую болезнь, но как созвездие симптомов, каждый из которых имеет дискретные нейронные корни.
Тем не менее, мы знаем, что кетамин работает быстрее, чем любой другой препарат, и эффективен для 65% пациентов, которые не реагируют на существующие методы лечения.
Так, кетамин может оказаться психиатрическим спасением с весьма удивительной историей. С 1962 года он был дежурным анестетиком для детей в пунктах неотложной помощи, поскольку быстро убивает боль, приглушает сознание и редко вызывает проблемы с дыханием или сердцем. Как говорилось в одном обзоре, дети под воздействием кетамина входят в «транс, подобный состоянию сенсорной изоляции», свободные от боли, памяти и сознания. Врачи скорой помощи полагаются на кетамин, уверенные в том, что в сознании или памяти детей не останется, например, травмы, которую они получили бы, когда им вправляли поврежденную руку.
С другой стороны, кетамин — известный рекреационный препарат, которым потенциально можно злоупотребить. Отключка, вызываемая умеренной дозой кетамина, сделала его популярным в клубах и на вечеринках с 1970-х годов, особенно в азиатских городах, таких как Гонконг. Его седативный эффект превратил «Special K» в наркотик для изнасилования. Врачи, пациенты и правительственные учреждения, спонсирующие исследования, часто с подозрением относятся к препарату, способному вызывать галлюцинации, как это было с такими психоделиками, как псилоцибин и экстази, несмотря на их потенциал для лечения депрессии или ощущения тревоги. Каждый из них, как и кетамин, имеет тенденцию демонстрировать быстрые результаты после однократного применения.
В 1999 году — в этом же году кетамин был объявлен в Соединенных Штатах контролируемым веществом — исследователи из Йеля обнаружили его действенный эффект как антидепрессанта. Команда, которую возглавили Денис Чарни (Dennis Charney), в настоящее время декан Школа медицины Икана Медицинского центра Маунт-Синай в Манхэттене, и Джон Кристал (John Krystal), ныне заведующий кафедрой психиатрии Йельского университета, использовала кетамин для изучения глутамата: поскольку было известно, что кетамин способен блокировать рецепторы глутамата, это могло показать, какую роль возбуждающие нейромедиаторы играют в мозге человека в состоянии депрессии. К их удивлению, они обнаружили, что после принятия препарата пациенты чувствуют себя лучше, часто на протяжении нескольких часов. Разовой дозы, гораздо меньшей, чем та, что использовалась для анестезии, как правило, хватало на несколько недель.
Начиная с 1999 года, эти результаты были воспроизведены в десятках исследований, где испытуемыми часто были те пациенты, которые не реагировали на другие препараты. Кетамин также работал в случае больных биполярным расстройством в депрессивных фазах, не вызывая мании, которая иногда возникала после классических антидепрессантов. Большинство страдающих депрессией людей, принимавших участие в исследовании, отреагировали на кетамин. Для пациентов с суицидальными наклонностями эта быстрая реакция может оказаться спасительной. Примерно 50 врачей в США в настоящее время предлагают вливания кетамина как средство от депрессии.
Многие эксперты в данной области рассматривают появление кетамина и будущих быстрых антидепрессантов, основанных на глутамате, как большой шаг вперед. «На мой взгляд, — недавно сказал NPR Санакора, — это самая захватывающая разработка в лечении аффективных расстройств за последние 50 лет».
Как кетамин, так и прежние антидепрессанты в качестве результата имеют более полные «деревья» нейронов, но приходят к нему разными путями, на разных скоростях. Эффект Prozac и прочих препаратов на основе серотонина проявляетcя через примерно четыре-шесть недель. Знаковое исследование Science 2003 года ученых Колумбийского университета Рене Хена (René Hen) и Рональда Думана (Ronald Duman, в настоящий момент работающего в Йельском университете), обнаружило, что антидепрессанты на основе серотонина работают только в том случае, если они стимулируют рождение новых нейронов в гиппокампе. Этим новым нейронам требуется от четырех до шести недель, чтобы созреть, примерно столько же времени, сколько нужно обычным антидепрессантам, чтобы поднять настроение подавленного человека. В исследовании 2010 года утверждается, что СИОЗС, подобные Prozac, могут функционировать, заглушая высвобождение глутамата в ответ на стресс. Таким образом, даже старые антидепрессанты, когда работают, могут воздействовать на систему глутамата.
Кетамин, с другой стороны, оказывает непосредственное действие на зрелые нейроны, удобряя их и делая более ветвистыми или защищая их от повреждений. Ключевой эффект кетамина состоит в том, чтобы блокировать глутаматные рецепторы одного типа. В результате в нейрон попадает меньше кальция, что снижает риск сжатия нейрона или его саморазрушения.
Сегодня психиатры и анестезиологи рекомендуют кетамин, цена которого варьируется между 300 и тысячей долларов за дозу, людям, крайне тяжело переносящим депрессию или страдающим от хронических болей. Страховка обычно не покрывает стоимость вливания, потому что, хотя кетамин и одобрен FDA в качестве анестезирующего средства, но не был утвержден в качестве антидепрессанта. Каждое новое применение препарата требует многофазных клинических испытаний для утверждения FDA, как правило, финансируемых фармацевтическими компаниями, которые не слишком расположены инвестировать в лекарство, которое они не могут превратить в деньги. Кетамин получил свой первоначальный патент в 1966 году, и его срок давно истек. Таким образом, даже если фармацевтические компании проведут кетамин через дорогостоящий процесс утверждения его в качестве антидепрессанта, врачи могут по-прежнему назначать дешевые генерические формы, уже доступные для анестезии, вместо дорогих патентованных версий, предназначенных для депрессии. Это старая история. Литий карбонат, который также действует на рецепторы глутамата, по-прежнему является одним из самых надежных препаратов для лечения биполярного расстройства. Но литий как элемент не может быть запатентован. Так, несмотря на свою эффективность, эти таблетки-синонимы притягивают совсем не много корпоративных долларов.
Жестокая правда об аффективных расстройствах заключается в том, что не все их формы излечимы. Топография головного мозга свидетельствует о структурных различиях между белым веществом у здоровых людей по сравнению больными биполярным аффективным расстройством. Различия в личностных качествах и фазах сна у этих больных также сохраняются, даже в периоды между маниакальными и депрессивными состояниями. Структурные изменения, по всей вероятности, имеют генетические корни, и если они однажды возникли, их трудно или даже невозможно обратить вспять.
Тем не менее, если препарат предотвращает проявления аффективного расстройства, он мог бы предотвратить возникновение вредных анатомических изменений. Так же, как вакцина вооружает организм против конкретного вируса, препарат, подобный кетамину, введенный до начала кризиса, вызывающего срыв, может защитить мозг от последствий стресса. Как и вакцину, этот препарат, возможно, потребуется дать всего один раз для обеспечения длительной защиты.
Первое свидетельство того, что кетамин может не только лечить людей, но и предотвращать аффективные расстройства, поступило с поля боя. Раненным в Ираке американским солдатам вводили различные анестетики, включая кетамин. Поскольку кетамин способен вызывать галлюцинации, хирурги были обеспокоены тем, что пациенты будут травмированы еще сильнее: страшные галлюцинации, связанные с боевыми действиями, могли вызвать у солдат более высокий риск психических заболеваний.
Но они обнаружили противоположные результаты. По имеющимся данным, из 25 тысяч военнослужащих, раненных в Ираке между 2002 и 2007 годом, те, кому вводили кетамин при лечении ожогов, зарегистрировали более низкие показатели посттравматического стрессового расстройства. Среди гражданских лиц и солдат, госпитализированных по причине ожогов, 45% в конечном итоге страдают посттравматическим стрессом. Между тем, среди тех солдат, которых на поле боя лечили препаратами с кетамином, лишь половина заболела этим недугом — даже если у них были более серьезные ожоги, требующие большого количества операций и длительного пребывания в больнице.

Ребекка Брахман (Rebecca Brachman), невролог, недавно защитившая докторскую диссертацию в Колумбийском университете, а также ее научный руководитель Кристин Денни (Christine Denny) проводили опыты, давая кетамин мышам, а затем подвергая их стрессам. Исследователи протестировали несколько типов стресса, в том числе тот, что возникает, когда на протяжении двух недель группа более агрессивных мышей «притесняет» остальных. После подобного рода ежедневной дедовщины у мышей как правило развивается посттравматический стресс, эквивалентный человеческому, и депрессия: замораживание в новом пространстве, отказ взаимодействовать с другими мышами и отсутствие движения в тесте на принудительное плавание. Однако мыши, получившие «прививку» до начала агрессии, показали гораздо лучшие результаты: впоследствии они не находились в состоянии депрессии. Брахман и Денни обнаружили, что защита от разовой дозы длилась на протяжении нескольких недель, несмотря на то кетамин находится в организме лишь в течение нескольких часов. Хотя они это еще не проверили, вполне возможно, что, как и вакцина, эта защита может длиться намного дольше. Результаты их опытов на грызунах дают право предположить, что кетамин эффективнее в качестве профилактического средства, а не антидепрессанта.
Денни говорит, что рано или поздно мы начнем использовать кетамин в плановом порядке для предотвращения ПТСР у участников боевых действий, жертв изнасилования или тех, кто пережил аварию или массовые расстрелы. По словам Брахман, кетамин, как кажется, выполняет у мышей защитную функцию гораздо лучше, когда его дают до стрессовых событий. Тот факт, что мы не в состоянии предсказать большинство травматических жизненных событий, ограничивает полезность препарата. Но при введении его после травмы, до того, как начнет сказываться психологический ущерб — как в случае с обожженными солдатами — кетамин все еще может выполнять защитную функцию. В настоящее время Денни исследует эту возможность.
А в ряде ситуаций насильственный шок предсказуем. «Мы не знаем, когда произойдет землетрясение, — говорит Брахман, — но нам известно, когда мы собираемся отправить работников ООН в районы, опустошенные стихийным бедствием». Когда люди знают, что им предстоит оказаться в высшей степени травматической ситуации, считает исследователь, профилактический препарат, введенный заранее, может защитить их мозг от длительных последствий стресса. Подумайте о рабочих, разбирающих завалы после землетрясения, о пожарных или спасателях в Сирии, выволакивающих искалеченных людей из-под обломков.
Идея о том, что одна инъекция может предотвратить аффективные расстройства, является радикальным отходом от принятого сегодня в психиатрии образа мышления. Но здесь есть и некоторые прецеденты: терапевтические беседы и медитация уже давно сосредоточены на повышении устойчивости к стрессу. Биполярные пациенты, например, принимают «нейропротекторные» препараты, такие как литий, не для того, чтобы лечить текущие симптомы, но для защиты от будущих кризисов.
Конечно, не все доверяют кетамину как безопасному средству. Нам ничего не известно о долгосрочной безопасности кетамина, говорит Нестлер. У пациентов с анестезией, принимавших гораздо большие дозы, не наблюдалось никаких продолжительных болезненных ощущений, но они не подвергались постоянному лечению, какое назначается при приеме антидепрессантов.
Кроме того, пошатнуть репутацию кетамина как уличного наркотика очень непросто. Многие врачи считают галлюцинации неприемлемым риском для пациентов, которые, как они опасаются, могут пристраститься к препарату. Санакора из Йельского университета отмечает, что его испытуемые, которые проходили обследование в связи с злоупотреблением наркотиками или алкоголем, часто находили ощущение отключки неприятным или тревожным. Психоделический опыт оказывается сюрреалистическим, отмечает он, он далек от млеющего удовольствия, получаемого от таких наркотиков, как алкоголь, Xanax или героин. Экстремальные отключки с кетамином, называемые падением в «K-дыру», часто сравнивают с состоянием, близким к смерти, или сбивающими с толка ощущениями выхода из собственного тела — большинству людей такая перспектива едва ли покажется радужной.
Но поскольку доза антидепрессанта намного ниже той, что необходима для наркотического опьянения, многие пациенты этого даже не замечают. Фармацевтические компании также конкурируют между собой, стремясь разработать менее «наркоманскую» альтернативу. Johnson & Johnson тестирует эскетамин в форме спрея для носа, это версия кетамина с меньшим психоактивным воздействием. Компания Naurex закончила вторую фазу испытаний Rapastinel, препарата, который, подобно кетамину, частично блокирует те же самые рецепторы глутамата, но не имеет психоделической природы.
Пионеры кетамина подчеркивают, что их профилактическое исследование открывает новый путь в науке, который вселят надежды, но не предлагает немедленного излечения. Брахман и Денни утверждают, что кетамин, возможно, не станет препаратом с широким применением. Подобно антитуберкулезным препаратам в 1950-е годы, положившим начало эре антидепрессантов, кетамин становится первопроходцем в этом новом классе средств для психиатрической профилактики. «Эта работа показывает нам, что мы можем вмешаться заранее и создать своего рода самоукрепляющуюся устойчивость к стрессу, — говорит Брахман. — Мы не знали об этом раньше, вот что важно. Все остальное — следует ли нам это использовать и каким образом — все это придет позднее».
Тейлор Бек — журналист в Бруклине. До написания этой статьи он работал в лабораториях визуализации мозга, изучая память, старение и состояния сна.
Библиография
1. Maxwell, R.A. & Eckhardt, S.B. Drug Discovery Humana Press, New York, NY (1990).
2. Kennedy, S.H., et al. Differences in brain glucose metabolism between responders to CBT and venlafaxine in a 16-week randomized controlled trial. American Journal of Psychiatry 164, 778-788 (2007).
3. Vogel, G. Depression drugs’ powers may rest on new neurons. Science 301, 757 (2003).
4. Brachman, R.A., et al. Ketamine as a prophylactic against stress-induced depressive-like behavior. Biological Psychiatry (2015). Retrieved from DOI: http://dx.doi.org/10.1016/j.biopsych.2015.04.022